A standardpotenciál meghatározása a cink példáján. A galváncella működése elektrolizáló cellaként Elektródreakciók standard- és formálpotenciálja - PDF Ingyenes letöltés

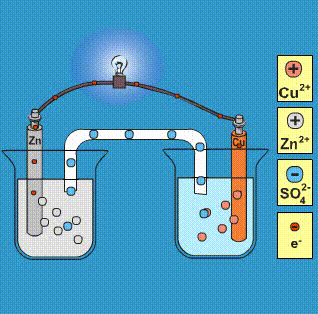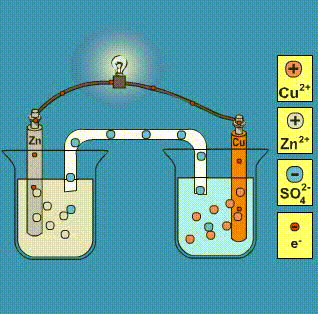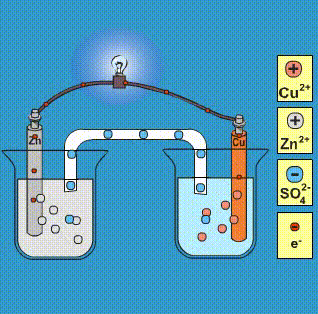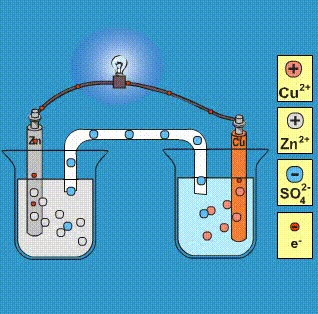
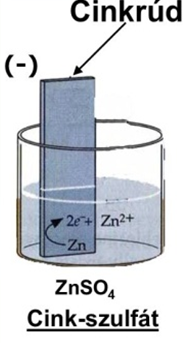
A standardpotenciál meghatározása a cink példáján. A galváncella működése elektrolizáló cellaként Elektródreakciók standard- és formálpotenciálja - PDF Ingyenes letöltés

A standardpotenciál meghatározása a cink példáján. A galváncella működése elektrolizáló cellaként Elektródreakciók standard- és formálpotenciálja - PDF Ingyenes letöltés
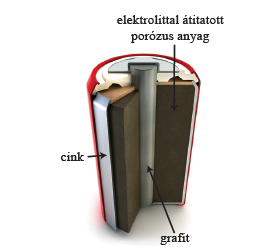
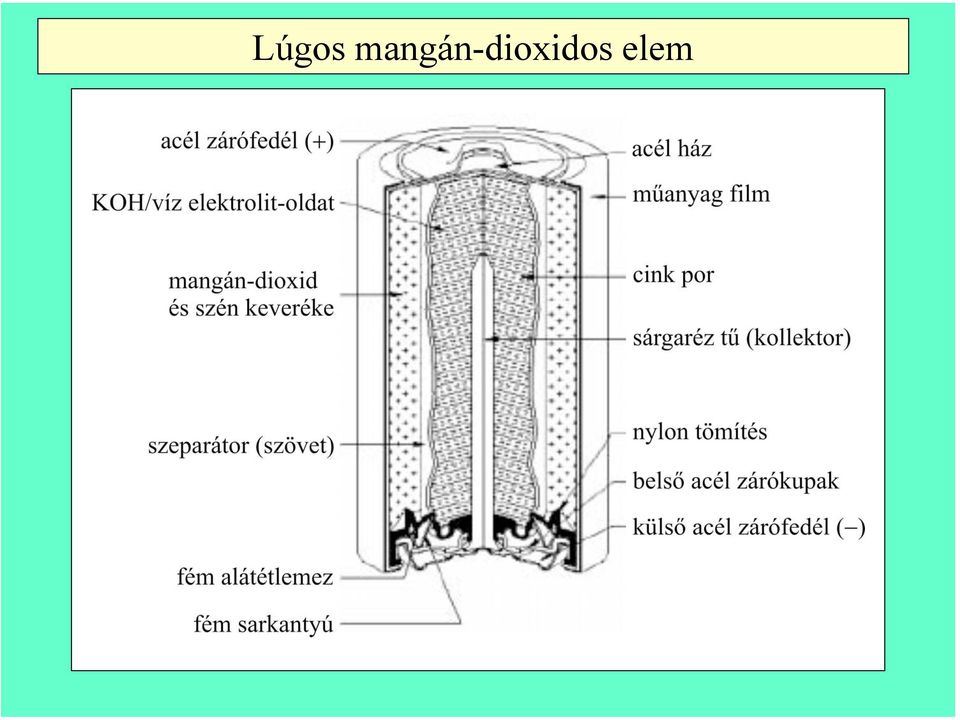
− C(s)|(s) MnO| Cl(aq) NH (aq), ZnCl | Zn(s) e2 (aq) Zn Zn(s) + → O(l) H MnOOH(s) e (aq) OH(s) MnO + →+ +
8.6.3.4.13. ábra: A Zn(OH)2, a Pb(OH)2 és a Sn(OH)2 csapadékok oldhatóságának logaritmusa a pH függvényében A diagram a
− C(s)|(s) MnO| Cl(aq) NH (aq), ZnCl | Zn(s) e2 (aq) Zn Zn(s) + → O(l) H MnOOH(s) e (aq) OH(s) MnO + →+ +